犬猫の毛包虫症(ニキビダニ症)って?原因・症状・治療・予防法まとめ【獣医皮膚科専門医が解説】

毛包虫症は小動物皮膚科臨床,特に犬の皮膚科診療において多く遭遇する皮膚疾患です。毛包に寄生する虫による皮膚病だから『毛包虫症』と言います。また、人ではニキビから検出される寄生虫である事から、『ニキビダニ』とも呼ばれています。毛包虫の特徴,発症要因,臨床症状を理解することは,毛包虫症の診断・治療を成功させるために不可欠です。この記事では犬と猫の毛包虫症について解説し,犬の毛包虫症に関しては2012年に発表された治療ガイドライン(※1)を参照しながら本症の診断および治療法について解説します。
■ 毛包虫とは?
毛包虫は多くの哺乳類の毛包内、また稀に脂腺や皮膚表層などに寄生するダニの一種です。毛包虫は、犬では生後数日において母親から授乳中の新生仔へ毛包虫が移行すると考えられています。毛包虫は卵性であり、虫卵、幼虫、若虫(第一および第二若虫)を経て成虫となります(図1)。

犬では、形態学的に異なる3種類の毛包虫が現在までに報告されています(※2、3)。最も一般的に分離されるDemodex canis(図1)、虫体の長い(D. canisの約2倍)D. injai(図2-a)、および虫体の短い(D. canisの約半分)名称未設定の毛包虫(図2-b)など、多様な種が存在します(※3)。D. canisが主に毛包内に寄生するのに対し、D. injaiは脂腺に、名称未設定の毛包虫は角質層に好んで生息するなど、種によって生息地が異なる傾向があります。
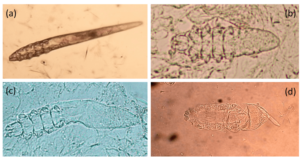
猫においても犬と同様に、現在までに3種類の毛包虫が報告されています。D. canisに形態が似るD. cati(図2-c)、体長が非常に短いD. gatoi(図2-d)、体長がD. canisより短くD. gatoiより長い名称未設定の毛包虫の3種が存在します。D. cati、名称未設定の毛包虫は毛包内に寄生するが、D. gatoiは角質層に寄生する傾向があります(※4)。また、D. gatoiは猫−猫間で接触感染すると考えられています(※5)。
■ 毛包虫症とは?
上記で紹介した毛包虫が過剰に増える事で引き起こされる皮膚病の事を『毛包虫症』と言います。毛包虫の過剰増殖により毛包が侵される疾患のため、臨床症状としては、主に毛穴に一致した皮膚症状が認められることが特徴となります。
1.犬の毛包虫症
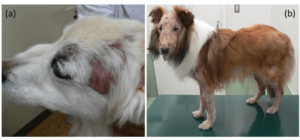
犬の毛包虫症は病変の範囲によって、限局性毛包虫症(図3-a)と全身性毛包虫症(図3-b)に区分されます。限局性と全身性の区分として、病変が4つ以下であり、かつ面積が2.5 cm以下であれば限局性と判断することが提唱されています。また、毛包虫症は発症年齢によって若年発症型と成年発症型に分類されます。若年発症型は3〜18ヶ月、成年発症型は4歳以上の発症とされるが、個々の症例において明確に分類することが困難な場合も多くあります。
①-1 若年発症型
若年発症型では、遺伝性、内部寄生虫症、栄養不良および衰弱が原因だと考えられてます(※6)。
②-1 成年発症型
成年発症型では内分泌疾患、腫瘍、化学療法、グルココルチコイド製剤の使用などによる後天的な免疫抑制状態が原因として考慮されています(※7-9)。しかし、これらの要因と毛包虫症の発症との間の具体的な病態機序に関しては明らかにされていません。
② 犬の毛包虫症の症状
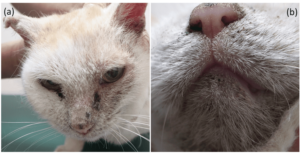
毛包虫症は毛包虫の過剰増殖により毛包が侵される疾患のため、主に毛穴に一致した皮膚症状が認められることが特徴となります。つまり脱毛、毛孔に一致したブツブツ(丘疹)/ニキビ(膿疱)/フケ(鱗屑)などのほか、赤み(紅斑)、黒ずみ(色素沈着)なども様々な程度で認められます(図4)。
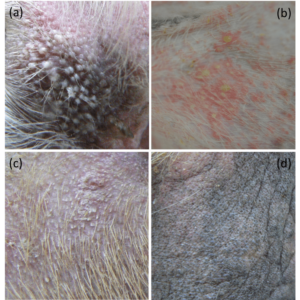
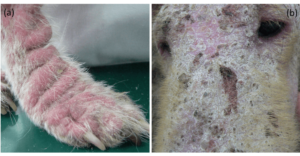
これらの症状は顔や前肢に発症することが多いとされています。全身性の毛包虫症においては、毛包の傷害/毛包炎が重度となると、毛包虫性のせつ腫症へと発展することがあります。せつ腫症では、結節〜腫瘤などの腫脹性病変、また排膿、出血などを伴ったびらん〜潰瘍性の病変を認めることがあります(図5)。せつ腫症を発症した場合は、毛包内に常在する細菌による二次感染を伴うことが多くあります。また、犬の毛包虫症ではかゆみを認めることは少ないとされています。
2. 猫の毛包虫症
猫の皮膚科診療において、毛包虫症と遭遇することは稀です。FIV(猫エイズ)、FeLV(猫白血病)の感染、糖尿病をはじめとした内分泌疾患、腫瘍、免疫抑制剤の使用などが発症要因として考慮されています。D. catiによる毛包虫症の場合、頭部や頚部を中心にに脱毛、毛包一致性の丘疹/鱗屑、紅斑などの皮疹を認めることが多いとされています(図6)。D. gatoiは皮膚表層に生息する毛包虫であるため、毛孔に一致する皮疹を認めることは少なく、一方で強い掻痒を伴うことが多いため、自己損傷性の脱毛、表皮剥離(びらん)、紅斑、毛包に一致しない鱗屑などの皮疹を認められます。
■ 毛包虫症の診断
①鑑別すべき皮膚疾患
第一に考慮しなければならない鑑別疾患としては、皮膚糸状菌症および細菌性毛包炎があげられます。これらの疾患は、毛包虫症と同様に毛包を侵す皮膚疾患なので、毛包虫症に類似した臨床症状を呈することがあります。
②皮膚掻爬物直接鏡検
毛包虫症は皮膚掻爬物直接鏡検により比較的簡便に診断することができます。皮膚掻爬物直接鏡検は、別名スクレイピングとも呼ばれる『皮膚を掘る』検査となります。外科用メスあるいは鋭匙という器具を用いて、被毛の走行に沿って、皮膚から出血が認められるまで深く掻爬を実施します。また、掻爬は複数箇所より行うことが望ましく、掻爬部位を指で絞ることは、ダニの検出率を向上させるために重要となります(※10)(図7a)。少し可哀想に思われるかもしれませんが、ダニを見逃してもっと可哀想な事にならないように、集中して検査を行います。
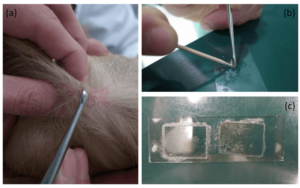
掻爬物はスライドグラス上に滴下したミネラルオイルやKOH溶液などと混和した後に顕微鏡で確認します(図7b)。正常皮膚から毛包虫が検出されることは極めて稀なため、この検査で1匹以上の毛包虫が確認されれば毛包虫症を疑います(※11)。また、ニキビダニの種類によっては、毛穴ではなく脂腺に生息する傾向があるため、この検査を行っても検出されない場合があります。毛包虫症を疑う症状が認められ、皮膚掻爬検査で虫体が検出できなかった場合は、皮膚生検を考慮する必要があります。また、治療前の皮膚掻爬物直接鏡検において毛包虫の数、成長の各ステージ(虫卵、幼虫、若虫、成虫;図1)を記録し、治療後に同部位から再度皮膚掻爬を行ってその組成を比較することは、施行している治療の効果を評価する上で極めて重要となります。治療後にもかかわらず皮膚掻爬物に虫卵、幼虫が認められれば、毛包虫の繁殖活動が未だ活発であると考えられ、薬剤の変更を検討します。
③抜毛検査
抜毛検査は皮膚掻爬物直接鏡検に代替する毛包虫の検出法となります(※11)。抜毛検査は出血を伴わないため、皮膚掻爬物直接鏡検と比較して侵襲性の低い検査となります。基本的には、解剖学的に皮膚の掻爬が困難な部位(眼や口周囲、趾間など)、病変部の疼痛が強い部位などに適応を考慮します。抜毛検査では複数箇所、またできるだけ多くの被毛を採取することが重要となります。しかし、抜毛検査で毛包虫が検出されなかった場合でも、毛包虫症を除外できないことに注意する必要があります。そのため、抜毛検査が陰性であったときは、皮膚掻爬物直接鏡検の実施を必ず考慮します(抜毛検査で毛包虫が見つかれば、皮膚掻爬物直接鏡検の必要はありません)。また、皮膚糸状菌の感染の有無を併せて確認します(検査前にウッド灯検査を実施すると良いとされています)。
④細胞診
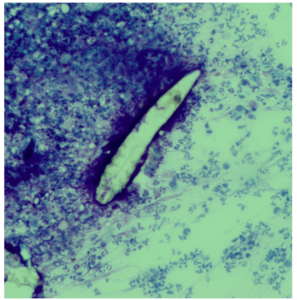
毛包虫の増殖が重度の場合、膿疱内容物、びらん〜潰瘍部の滲出液などのガラス直接押捺塗抹検査で虫体が検出されることがあります(図8)。毛包虫症と診断された場合には、2次的な細菌感染の存在を細胞診で確認することも重要です。毛包虫症に併発する細菌感染は主にブドウ球菌であるStaphylococcus pseudintermediusが一般的ですが、時にグラム陰性桿菌(Eshelichia coli、Pseudomonas aeruginosaなど)の感染が起こることがあるため、細菌感染の所見が細胞診で認められた場合は、細菌培養同定検査および薬剤感受性検査の実施を考慮します。
⑤皮膚生検
前述の通り、毛包虫症を疑う症状が認められたにも関わらず、毛包虫が検出されない場合、皮膚生検を考慮する必要があります。また、重度のせつ腫症により結節性〜腫瘤性病変を呈する症例では、深在性細菌/真菌感染症、脂肪織炎、異物、腫瘍などを除外するために皮膚生検の実施が望ましいとされています。
■ 犬の毛包虫症の治療
毛包虫症を治療するにあたって、発症年齢(若年 or 成年)および範囲(限局性 or 全身性)を第一に考慮します。若年発症および限局性毛包虫症は自然治癒する傾向にあるため、シャンプーなどの外用剤のみで奏功すし、内服や注射などによる駆虫治療を必要としない場合があります。しかし、限局性から全身性毛包虫症への移行、重度で長期間持続する若年発症性毛包虫症も時に認められるため、臨床経過を慎重にモニタリングする必要があります。成年発症・全身性毛包虫症に対しては単に毛包虫の駆虫のみではなく、2次的な細菌感染のコントロール、発症要因の探索・治療などを含め多面的にアプローチを行うことが重要です。
① 抗菌療法による細菌の2次感染のコントロール
細胞診において、毛包虫症の症例の皮膚病変部から細菌の2次感染が確認された場合には、適切な抗菌療法(抗生物質の全身投与、シャンプーなどの外用療法など)を併用することが必要となります。抗生物質の全身投与を行う際には、治療開始前に細菌培養同定・薬剤感受性検査を行うことが望ましい。特に細胞診においてグラム陰性桿菌の感染を示唆する所見が得られた場合は積極的に検査を実施する事が推奨されます。抗菌療法は細胞診で細菌感染を示唆する所見が消失するまで、最低でも2〜3週間継続する事が推奨されます。
②シャンプー療法
シャンプー療法は抗菌作用のみならず、皮膚に付着した鱗屑や痂皮などの除去のほか、物理的に毛包虫の数を減らすことが期待できます。一般的には過酸化ベンゾイル、クロルヘキシジン、硫黄・サリチル酸などを含有したシャンプー剤が用いられます。過酸化ベンゾイルおよび硫黄・サリチル酸シャンプーは脱脂作用があるため、シャンプー後の皮膚の過剰な乾燥を引き起こすので、充分保湿をするように心掛けましょう。
③薬剤による治療
1.アミトラズ
アミトラズによる外用療法は毛包虫症に対する治療法として多くの国で認可され、治療高価に関する報告が数多くあります(※12)。しかし、成年発症型毛包虫症では効果が低いと考えられています。中〜長毛種においてアミトラズによる外用療法を行う際には、毛刈りを行うことが推奨されています(※13)。アミトラズは溶液に病変部を浸すか、スポンジなどを用いて優しく皮膚病変部に塗布し、塗布後は風乾を行います。アミトラズの有害反応として、沈鬱、嗜眠、運動失調、過食、多飲、嘔吐、下痢などが報告されています。
2.ミルベマイシンオキシム
ミルベマイシンオキシムはいくつかの国において毛包虫症の治療薬として認可されています。しかし、成年発症型の毛包虫症に対しては本剤の治療効果は低いとされています(※14)。また、コリー犬にミルベマイシンオキシムを2.5 mg/kg、 24時間毎にて10日間経口投与した結果、投与による有害反応が認められなかった報告があります。
3. イベルメクチン
イベルメクチンは毛包虫症の治療薬として認可されていません。多くの研究においてイベルメクチンの治療効果が検討され、 24時間毎の経口投与による治療が推奨されています(※15-19)。イベルメクチン投与により嗜眠、振戦、散瞳などの神経症状が起こる可能性、また感受性の高い個体では時に死亡する可能性があります。コリー種においてこれらの有害反応が出る可能性が高いですが、他の犬種でも有害反応の報告があります(※20)。また、MDR1遺伝子変異のある個体では急性毒性が発生する可能性が高いため、使用は避ける事が推奨されています(※21-23)。MDR1遺伝子変異の有無は血液検査でチェック可能である為、投与前に変異の有無を確認する事が推奨されています。
投与法としては、徐々に投与量を増加しながら有害反応の発生をモニタリングすることが推奨されています。また、ケトコナゾールやシクロスポリンなどのP糖タンパク阻害作用をもつ薬物の併用は、有害反応が起こる確率を高めるため注意が必要となります(※24,25)。有害反応が認められた場合は速やかにイベルメクチンの投与を中止します。
4.モキシデクチン
モキシデクチンは、24時間毎、経口投与による治療が推奨されています。(※26,27)。モキシデクチンによる有害反応はイベルメクチンと同様のものが報告されているが、イベルメクチンよりも発生率が高いとされています。イベルメクチン同様、MDR1遺伝子変異のある個体に対する使用は避けるべきとされています。投与法はイベルメクチンと同様に低容量から開始し、徐々に用量を増量します。
モキシデクチンを含むスポットオン製剤による治療も報告されており、若年発症型で比較的軽症例に対し週1回の投与が推奨されています。(※28,29)。スポットオン製剤による治療は投与開始2〜3週間で効果が認められなかった場合、他の治療への変更を考慮することが推奨されています。
5.ドラメクチン
ドラメクチンの毛包虫症への治療効果に関する報告は少ない。過去の2つの報告から判断すると、 1週間に1回、皮下注射あるいは経口投与が毛包虫症の治療に推奨されています(※30,31)。しかし、成年発症型では治療後の再発率が高いとされています。有害反応としてはイベルメクチンと同様に神経症状が一般的であり、MDR1遺伝子変異のある個体に対する使用は避けるべきです。
6.その他の治療
昨今、セラメクチンの1週間に1回あるいは1ヶ月に2回の経口投与による治療が報告されたが、全身性の毛包虫症に対する治療成功率は低いとされています(※32)。その他、アミトラズのカラー、ビタミンE、ハーブやホメオパシーなどによる治療報告があるが、その治療エビデンスは乏しいとされています。
■ 猫の毛包虫症の治療
猫の毛包虫症は発生率が低いため、犬と比較すると治療に関する大規模な研究報告は少ない。犬と同様に、背景となる発症要因を精査することは極めて重要である。また、D. gatoiに関しては猫−猫間で伝染する可能性があるため、同居猫がいる場合にはそれらに対する治療を行う必要があります。
1.石灰硫黄混合剤による治療
過去の報告からは、石灰硫黄混合剤による外用療法が良い治療成績を残しています(※34-36)。石灰硫黄混合物の5〜7日おきの外用療法により毛包虫症に罹患した猫(D. cati 8頭、D. gatoi 16頭)の約92%(22/24)が4〜6週で臨床症状が改善したという報告があります。また、これらの症例で副作用は認められていまsん。石灰硫黄混合物の使用の際は、製剤を舐めとることによる口腔内潰瘍や消化器症状が発生する可能性があるため、エリザベスカラーを装着することが望ましいとされています(※37)。
2.アミトラズ
アミトラズの外用療法(週2回〜2週間に1回)では毛包虫症に罹患した13頭の猫(D. cati 11頭、D. gatoi 2頭)のうち11頭の猫(全てD. catiの症例)において改善が認められたと報告されています(※38-41)。副作用として沈鬱、流唾症が1頭において認められています。
3. ドラメクチン
3頭の毛包虫症に罹患した猫(全てD. cati)にドラメクチンを1週間に1回、皮下注射による治療を行ったところ、合計2〜3回の投与で3頭全ての猫で改善が認められています(副作用は認められていない)(※42)
■ 毛包虫症の治療期間および予後
犬の毛包虫症の予後は比較的良好です。発症要因となる基礎疾患のコントロールが難しい場合は治療が長期化し、時に完全な治癒が期待できない場合もあります。また、一旦症状が良くなった後でも、1〜2年以内に再発した症例が少数報告されています。治療を行うにあたって、どの程度の治療期間を要するのかを理解することは非常に重要となります。治療の継続・終了を決定するための指標としては皮膚掻爬物直接鏡検を用います。臨床症状の改善をもって治療終了を決定することは危険であり、再発リスクになるため気を付けましょう。治療後に皮膚掻爬を行って毛包虫が検出されなかった場合、さらに治療を継続して1ヶ月おきに2回の皮膚掻爬を行います。この2回の皮膚掻爬で共に毛包虫が確認されなかった際に治療終了と判定することが推奨されます。掻爬する部位としては、初診時に最も重度であった病変部より3〜5箇所行うことが望ましいとされています。治療修了後から12ヶ月間は臨床症状の再発の有無を定期的にモニターすることが重要になります。一見しつこいように思われるかもしれませんが、それ程再発しやすい皮膚病という事です。
■ 毛包虫症の予防法
一番の予防法は、発症要因の探索を行う事です。成年発症型の毛包虫症では、血液学的検査、尿検査、画像検査などをはじめとした各種臨床検査を用いて、内分泌疾患や腫瘍などの存在を探索しましょう。特に甲状腺機能低下症および副腎皮質機能亢進症の探索は入念に行うべきとなります。また、化学療法(抗がん剤)やグルココルチコイド製剤(ステロイド剤)、その他免疫抑制剤による治療歴、内部寄生虫の感染、給餌の質や量も発症要因となるので意識しましょう。発症要因が特定できた場合は、毛包虫症の治療に加えてそれらに対するアプローチを並行して実施します。発症要因が特定できなかった場合でも、定期的に臨床症状のモニタリングや各種検査を行うことが重要となります。
■ おわりに
毛包虫症を治療するにあたって、何よりも飼い主さんの理解と協力が必要であると感じています。今回概説した毛包虫症の特徴、診断、治療の基本事項を双方が理解した上で、本症がどのような病気で、それぞれの治療がどの程度の効果があり、どの程度治療期間がかかるのかを理解し、協力して治療を進める事が完治させる秘訣だと考えています。治療が長期化すると飼い主さんが不信感や不安を抱く場合も少なくありませんが、獣医師とコミュニケーションを取り合って、粘り強く治療を行いましょう!心配な事や不安な事があれば、お気軽にご質問ください。
■ 参考文献リスト
- Mueller、 R.S.、 Bensignort、 E.、 Ferrer、 L.、 Holm、 B.、 Lemarie、 S.、 Paradis、 M.、 Shipstone、 A. (2012): Treatment of demodicosis in dogs: 2011 clinical practice guidelines. Veterinary Dermatology、 23: 86-96.
- Chesney、 C.J. (1999): Short form of Demodex species mite in the dog: occurrence and measurements. Journal of Small Animal Practice、 40: 58-61.
- Desch、 C.E.、 Hillier、 A. (2003): Demodex injai: a new species of hair follicle mite (Acari: Demodecidae) from the domestic dog (Canidae). Journal of Medical Entomology、 40: 146-149.
- Conroy、 J.D.、 Healey、 M.C.、 Bane、 A.G. (1982): New Demodex sp. infesting a cat: a case report. Journal of the American Animal Hospital Association、 18: 405-407.
- Foley、 R.H. (1995): Feline demodicosis. Compendium on Continuing Education for the Practicing Veterinarian、 17: 481-487.
- Plant、 J.D.、 Lund、 E.M.、 Yang、 M. (2011): A case–control study of the risk factors for canine juvenile-onset generalized demodicosis in the USA. Veterinary Dermatology、 22: 95-99.
- Duclos、 D.D.、 Jeffers、 J.G.、 Shanley、 K.J. (1994): Prognosis for treatment of adult-onset demodicosis in dogs: 34 cases (1979–1990). Journal of the American Veterinary Medical Association、 204: 616-619.
- Lemarie、 S.、 Hosgood、 G.、 Foil、 C.S. (1996): A retrospective study of juvenile and adult-onset generalized demodicosis in dogs (1986–1991). Veterinary Dermatology、 7: 3–10
- Miller、 W.H. Jr、 Scott、 D.W.、 Wellington、 J.R. Panic、 R. (1993): Clinical efficacy of milbemycin oxime in the treatment of generalized demodicosis in adult dogs. Journal of the American Veterinary Medical Association、 203: 1426–1429.
- Beco、 L.、 Fontaine、 F.、 Bergvall、 K.、 Favrot、 C. (2007): Comparison of skin scrapes and hair plucks for detecting Demodex mites in canine demodicosis、a multicentre、 prospective study. Veterinary Dermatology、 18: 381 (Abstract).
- Mueller、 R.S.、 Bettenay、 S.V. (2011): Skin scrapings and skin biopsies. In: Textbook of Veterinary Internal Medicine. (Ettinger、 S.J.、 Feldman、 E.C.、 ed.)、 368–371、 Saunders、 Philadelphia.
- Mueller、 R.S. (2004): Treatment protocols for demodicosis: an evidencebased review. Veterinary Dermatology、 15: 75–89.
- Hugnet、 C.、 Bruchon-Hugnet、 C.、 Royer、 H.、 Bourdoiseau、 G. (2001): Efficacy of 1.25% amitraz solution in the treatment of generalized demodicosis (eight cases) and sarcoptic mange (five cases) in dogs. Veterinary Dermatology、 12: 89–92.
- Holm、 B.R. (2003): Efficacy of milbemycin oxime in the treatment of canine generalized demodicosis: a retrospective study of 99 dogs (1995–2000). Veterinary Dermatology、 14: 189–195.
- Fondati、 A. (1996): Efficacy of daily oral ivermectin in the treatment of 10 cases of generalized demodicosis. Veterinary Dermatology、 7: 99–104.
- Ristic、 Z.、 Medleau、 L.、 Paradis、 M.、 White-Weithers、 N.E. (1995): Ivermectin for treatment of generalized demodicosis in dogs. Journal of the American Veterinary Medical Association、 207: 1308–1310.
- Guaguere、 E. (1996): Traitement de la demodecie generalisee du chien par l’ivermectine: a propos de 20 cas. Pratique Medicale et Chirurgicale de l’Animal de Compagnie、 31: 31–40.
- Medleau、 L.、 Ristic、 Z.、 McElveen、 D.R. (1996): Daily ivermectin for the treatment of generalized demodicosis in dogs. Veterinary Dermatology 7: 209–212.
- Mueller、 R.S.、 Hastie、 K.、 Bettenay、 S.V. (1999): Daily oral ivermectin for the treatment of generalised demodicosis in 23 dogs. Australian Veterinary Practitioner、 29: 132–136.
- Mueller、 R.S.、 Bettenay、 S.V. (1999): A proposed new therapeutic protocol for the treatment of canine mange with ivermectin. Journal of the American Animal Hospital Association、 35: 77–80.
- Mealey、 K.L.、 Bentjen、 S.A.、 Gay、 J.M.、 Cantor、 G.H. (2001): Ivermectin sensitivity in collies is associated with a deletion mutation of the mdr1 gene.Pharmacogenetics、 11: 727–733.
- Mealey、 K.L.、 Meurs、 K.M. (2008): Breed distribution of the ABCB1-1D(multidrug sensitivity) polymorphism among dogs undergoing ABCB1 genotyping. Journal of the American Veterinary Medical Association、 233: 921–924.
- Roulet、 A.、 Puel、 O.、 Gesta、 S.、 Lepage、 J.F.、 Drag、 M.、 Soll、 M.、 Alvinerie、 M.、 Pineau、 T. (2003): MDR1-deficient genotype in Collie dogs hypersensitive to the P-glycoprotein substrate ivermectin. European Journal of Pharmacology、 460: 85–91.
- Hugnet、 C.、 Lespine、 A.、 Alvinerie、 M. (2007): Multiple oral dosing of ketoconazole increases dog exposure to ivermectin. Journal of Pharmacy and Pharmaceutical Sciences、 10: 311–318.
- Mayer、 U.K.、 Glos、 K.、 Schmid、 M.、 Power、 H.T.、 Bettenay、 S.V.、 Mueller、 R.S. (2008): Adverse effects of ketoconazole in dogs – a retrospective study. Veterinary Dermatology、 19: 199–208.
- Bensignor、 E.、 Carlotti、 D. (1998): Moxidectin in the treatment of generalized demodicosis in dogs. A pilot study: 8 cases. In: Advances in Veterinary Dermatology. (Kwochka K.W.、 Willemse、 T.、 Von、 Tscharner、 C.、 eds.)、 554–555、 Butterworth-Heinemann、 Oxford.
- Wagner、 R.、 Wendlberger、 U. (2000): Field efficacy of moxidectin in dogs and rabbits naturally infested with Sarcoptes spp.、 Demodex spp. and Psoroptes spp. mites. Veterinary Parasitology、 2000; 93: 149–158.
- Paterson、 T.E.、 Halliwell、 R.E.、 Fields、 P.J.、 Louw、 M.L.、 Louw、 J.P.、 Ball、 G.S.、 Pinckney、 R.D.、 McKibben、 J.S. (2009): Treatment of caninegeneralized demodicosis: a blind、 randomized clinical trial comparing the efficacy of Advocate_ (Bayer Animal Health) with ivermectin. Veterinary Dermatology、 20: 447–455.
- Mueller、 R.S.、 Meyer、 D.、 Bensignor、 E.、 Sauter-Louis、 C. (2009): Treatment of canine generalized demodicosis with a ‘spot-on’ formulation containing 10% moxidectin and 2.5% imidacloprid (Advocate、 Bayer Healthcare). Veterinary Dermatology、 20: 441–446.
- Johnstone、 I.P. (2002): Doramectin as a treatment for canine and feline demodicosis. Australian Veterinary Practitioner、 32: 98–103.
- Murayama、 N.、 Shibata、 K.、 Nagata、 M. (2010): Efficacy of weekly oral doramectin treatment in canine demodicosis. Veterinary Record、 167: 63–64.
- Schnabl、 B.、 Bettenay、 S.、 Glos、 N.、 Linek M.、 Loewenstein、 C.、 Mueller、 R.S. (2010): Oral selamectin in the treatment of canine generalised demodicosis. Veterinary Record、 166: 710–714.
- Cowan、 L.A.、 Campbell、 K. (1988): Generalized demodicosis in a cat responsive to amitraz. Journal of the American Veterinary Medical Association、 192: 1442–1444.
- Morris、 D.O. (1996): Contagious demodicosis in three cats residing in a common household. Journal of the American Animal Hospital Association、 32: 350–352.
- Morris、 D.O.、 Beale、 K.M. (2000): Feline demodicosis. In: Kirk’s Current Veterinary Therapy XIII、 (Bonagura、 J.D.、 ed.)、 580–582、 W.B. Saunders、 Philadelphia.
- Chalmers、 S.、 Schick、 R.O.、 Jeffers、 J.G. (1989): Demodicosis in two cats seropositive for feline immunodeficiency virus. Journal of the American Veterinary Medical Association、 194: 256–257.
- Moriello、 K.A.、 DeBoer、 D.J. (1995): Feline dermatophytosis: recent advances and recommendations for therapy. In: Feline Dermatology、 (Kunkle、 G.A.、 ed.)、 901–22、 W.B. Saunders、 Philadelphia.
- Cowan、 L.A.、 Campbell、 K. (1988): Generalized demodicosis in a cat responsive to amitraz. Journal of the American Veterinary Medical Association、 192: 1442–1444.
- Stogdale、 L.、 Moore、 D.J. (1982): Feline demodicosis. Journal of the American Animal Hospital Association、 18: 427–432.
- Wilkinson、 G.T. (1983): Demodicosis in a cat due to a new mite species. Feline Practice、 13: 6.
- Yathiraj、 S.、 Rai、 M.T.、 Rao、 P.M. (1994): Treatment of generalized demodicosis in a cat – a case report. Indian Veterinary Journal、 71: 393–395.
- Johnstone、 I.P. (2002): Doramectin as a treatment for canine and feline demodicosis. Australian Veterinary Practitioner、 32: 98–103.








この記事へのコメントはありません。